Célula a Combustível (Fuel Cell) é uma tecnologia que utiliza a combinação química entre oxigênio e hidrogênio para gerar energia elétrica, energia térmica (calor) – e água. Além das várias tecnologias existentes para combinar esses dois elementos, existem várias fontes de hidrogênio a serem utilizadas pelas CaCs, tais como a gasolina, o gás natural, o óleo diesel, o etanol (álcool), o metanol, o lixo urbano e rural, a água, entre outros, onde se pode extrair e utilizar o hidrogênio para reagir com o oxigênio do ar.
As diferentes tecnologias de célula a combustível têm basicamente o mesmo princípio. São compostas por dois eletrodos porosos: o ânodo (terminal negativo) e o cátodo (terminal positivo), cada um revestido num dos lados por uma camada de catalisador de platina ou níquel, e separados por um eletrólito (material impermeável que permite movimento aos íons positivos – prótons – entre os eletrodos).
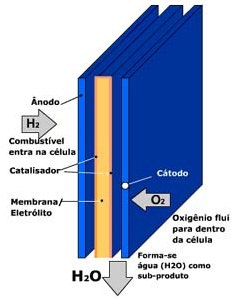
Dentro da Célula a Combustível

Ânodo
O terminal negativo – ânodo – tem canais de fluxo que distribuem o gás hidrogênio sobre a superfície do catalisador.
Catalisador
Uma fina camada de catalisador recobre o eletrólito ou membrana. O catalisador é um metal, normalmente platina ou níquel, que acelera as reações químicas entre o oxigênio e o hidrogênio.
Membrana ou Eletrólito
Algumas células utilizam eletrólitos líquidos e outras sólidas, como as membranas plásticas de troca de prótons para conduzirem cargas positivas, os prótons. Somente as cargas positivas atravessam o eletrólito, os elétrons não.
Cátodo
O terminal negativo – ânodo – tem canais de fluxo que distribuem o gás hidrogênio sobre a superfície do catalisador, e remove a água produzida durante a reação.
Dentro da célula a combustível, o gás hidrogênio pressurizado é bombeado para o terminal negativo, o ânodo. O gás é forçado a atravessar o catalisador.
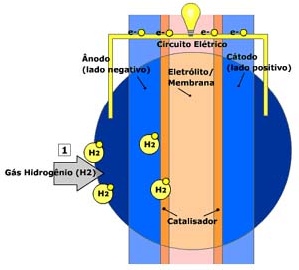
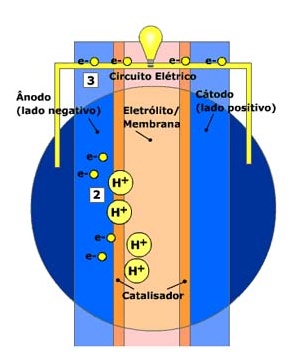
Quando a molécula de hidrogênio entra em contato com o catalisador, ela se separa em dois íons de hidrogênio (H+) e dois elétrons (e-).
Os elétrons (e-) são conduzidos através do ânodo, contornando o eletrólito até atingirem o circuito externo, onde acendem uma lâmpada ou motor elétrico, e retornam para o terminal positivo, o cátodo. O fluxo de elétrons é a corrente elétrica.
Reação Química
2H2 => 4H+ + 4e-
O oxigênio (O2), retirado do ar, entra na célula a combustível pelo terminal positivo, o cátodo. O gás é forçado a se dispersar no catalisador.
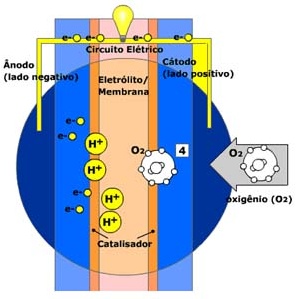
O catalisador separa a molécula de oxigênio em dois átomos de oxigênio.
Cada átomo de oxigênio atrai dois íons H+ através do eletrólito.
Estes dois íons H+ combinam com o átomo de oxigênio e dois elétrons provenientes do circuito externo, para formar a molécula de água (H2O). Nesta reação, uma certa quantidade de calor é liberada.
Reação Química:
O2 + 4H+ + 4e- => 2H2O
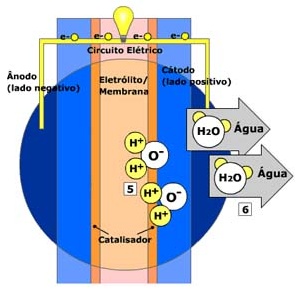
Explicação mais detalhada
Na maioria das células a combustível, o ânodo é alimentado com hidrogênio – combustível -, onde ocorre a ionização deste, por reação catalítica na platina, convertendo o hidrogênio H2 em prótons H+ e elétrons H-.
O cátodo é alimentado pelo oxigênio – o oxidante – retirado do ar. Os elétrons circulam por um circuito externo gerando uma corrente elétrica no sentido do cátodo, o terminal positivo.
Os prótons atravessam o eletrólito – que pode ser líquido ou sólido – no sentido do cátodo também. No cátodo, o elétron e o próton reagem com o oxigênio, retirado do ar, formando moléculas de água e liberando calor devido à reação exotérmica. Tem-se então, vapor d’água.
O vapor quente pode ser utilizado para aquecimento, ou ser integrado à uma turbina a vapor para gerar mais eletricidade. Pode também ser utilizado para gerar hidrogênio novamente através da eletrólise (quebra da molécula de água em hidrogênio e oxigênio) utilizando um painel solar, por exemplo (CaCs Regenerativas).
Muitas vezes o hidrogênio utilizado pela célula a combustível não está na sua forma mais pura, H2. Ele está misturado a outros elementos presentes num combustível, tal como o gás natural, a gasolina e o álcool (etanol), e tem que ser retirado. Para extrair o hidrogênio é utilizado um reformador.
Em algumas tecnologias de células a combustível, devido à alta temperatura de operação, entre 600°C e 1000°C, a reforma do combustível é feita internamente. Já em outras tecnologias, que atuam em temperaturas mais baixas, é necessário um reformador, o que implica em custos adicionais.
Fonte: Brasil H2 Fuel Cell Energy
Por: Eng. Emilio Hoffmann Gomes Neto





